遺伝情報継承に重要な染色体領域を維持する仕組みを解明~がん化プロセスの理解やその治療への貢献に期待~
【ポイント】
- 隣り合った異なるクロマチン構造を分ける仕組みを解明。
- この仕組みが破たんすると遺伝情報が次世代へ安定に継承されないことを確認。
- CENP-Aの異所的局在を標的とする新たながん治療薬の開発に期待。
【概要】
北海道大学大学院理学研究院の村上 洋太 教授及び常峰 悟 学術研究員らの研究グループは、遺伝情報を継承するために重要な染色体領域を安定に維持する仕組みの一端を明らかにしました。
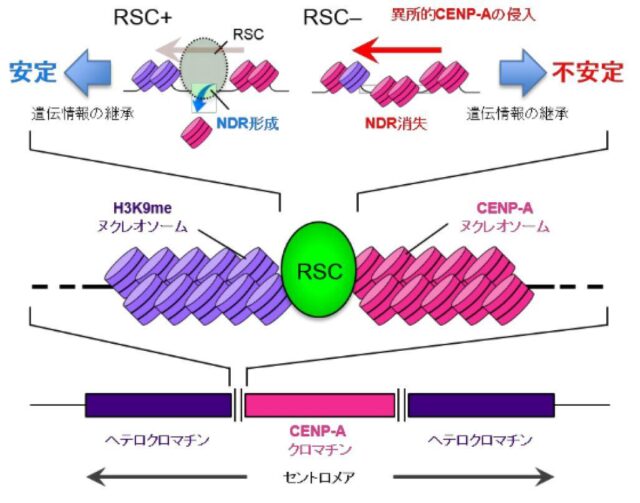
セントロメアは染色体を正確に分配するうえで最も重要な染色体領域です。セントロメアは、2つの異なるクロマチン構造から構成されており、内側領域にはCENP-Aタンパク質で規定されるCENP-Aクロマチンが、外側領域にはヒストンH3の9番目のリジンのメチル化で規定されるヘテロクロマチンが形成されます。2つのクロマチン構造の境界は厳密にその場所が決まっていますが、それがどのようにして形成されるのか、そのメカニズムの詳細は分かっていませんでした。
研究グループは、クロマチン関連の多くのプロセスで重要な役割を果たしているクロマチンリモデラーの1つ、RSC(Remodeling the Structure of Chromatin)の機能に着目し、分裂酵母を用いてRSCと境界形成との関係を遺伝学的・生化学的に解析しました。その結果、RSCは境界領域でCENP-Aクロマチンがヘテロクロマチンへ侵入するのを防いでいること、また、このCENP-Aの異常拡張により染色体の次世代への正確な継承が損なわれることが明らかになりました。さらなる解析から、RSCは境界領域にヌクレオソーム欠失領域(Nucleosome-Depleted Region, NDR)の形成を誘導し、このNDRがCENP-Aクロマチンとヘテロクロマチンの境界として機能することが分かりました。
近年、様々ながん細胞で、セントロメア以外の染色体領域にCENP-Aの異所的局在がみられることが報告されており、それに伴う染色体の不安定化とがん化との関係が注目されています。一方、RSCを含むクロマチンリモデラーの変異は様々ながんで見つかることから、これらはがん抑制因子として働くことが分かっています。本研究により、クロマチンリモデラーの変異によるがん化の原因がCENP-Aの異所的局在である可能性が示されました。この研究結果は、がん化の原因に対する理解に寄与するとともに、このシステムを標的とした新たながん治療薬の開発などにも発展することが期待されます。
なお、本研究成果は、2022年10月6日(木)にNucleic Acids Research誌でオンライン公開されました。
論文名:The chromatin remodeler RSC prevents ectopic CENP-A propagation into pericentromeric heterochromatin at the chromatin boundary(クロマチンリモデラーRSCはペリセントロメリックヘテロクロマチンへの異所的CENP-A侵入をクロマチン境界上で阻止する)
URL:https://doi.org/10.1093/nar/gkac827
詳細はプレスリリースをご覧下さい。